Вакцины от COVID-19 – фактчек
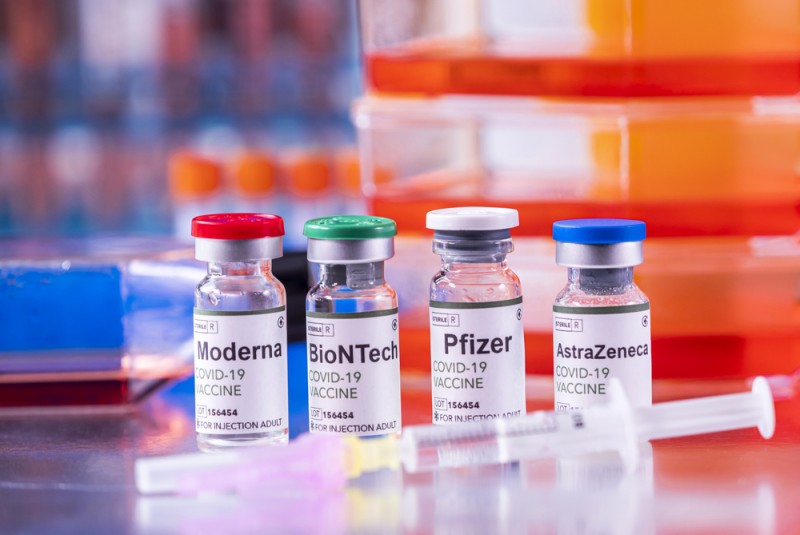
3 марта Мелинда Симмонс, посол Великобритании в Украине, написала твит следующего содержания: «Вакцины: фактчек. Вакцина от COVID-19 Covishield и Oxford-AstraZeneca AZD1222 являются идентичными. Covishield – это лицензированное название AZD1222, произведенной в Индии. Предположение, что вакцины AZ/Covishield, которые используются в Украине, отличаются по формуле, категорически неверно»1.
Такой твит госпожу посла заставил написать скандал, который разворачивается вокруг Covishield – вместо обещанной вакцинации «одними из первых в мире» вакциной производства Пфайзер и оригинальной вакциной АстраЗенека МОЗУ начало вакцинацию с огромным опозданием, да еще и ухитрилось привезти вакцину, произведенную на индийских фарммощностях.
При этом жители Украины не единственные, кто вслух выразил свое недоверие – аналогичные голоса раздаются и в ЕС, который настаивает на поставках оригинальной АстраЗенека2, и в Канаде, единственной из G7, которая на данный момент авторизовала Covishield, и в Великобритании, и даже в самой Индии3.
В этой статье мы попытаемся рассмотреть эти две вакцины поближе и отсеять истерику и страхи от реальной информации.
Генерик и генерики
Когда-то, в статье «Генерики – плоть от плоти или седьмая вода на киселе?» мы знакомили читателя с тем, чем отличаются генерические препараты (генерики, дженерики) от оригинальных.
Если суммировать вкратце, генерик – это фармацевтический продукт, который, как подразумевается, равнозначен оригинальному лекарственному средству, произведен без лицензии компании-оригинатора и продается после истечения срока действия патента или других исключительных прав. Такой продукт должен быть «существенно схожий с оригинальным продуктом, представленный в той же лекарственной форме, имеющий тот же качественный и количественный состав активных ингредиентов и такую же биоэквивалентность, что и оригинальный продукт» (Decree Number 97-221. 13 March 1997).
То есть и оригинал, и генерик должны быть представлены одним и тем же действующим веществом (например, ампициллина тригидратом) в одной и той же дозе и в одной и той же форме (таблетки, мазь и так далее), а также с одинаковой скоростью и в одинаковой степени всасываться и распределяться в органах и тканях при приеме одним и тем же путем, в одинаковых дозах и лекарственных формах (так называемая биоэквивалентность).
С последним пунктом обычно связывают все проблемы генериков. Часть из них может нарушать рецептуру вспомогательных веществ – то есть того, что стабилизирует, высвобождает действующее вещество из таблетки и вообще держит ее форму (например антидепрессант ТЕВА быстро сбрасывал дозу и из-за того приводил к депрессиям), часть – содержать примеси (как в случае с китайским свиным гепарином, содержавшим гиперсульфатированный хондроитинсульфат, резко усиливающий кровоточивость), а часть – как происходило в описанных Кэтрин Ибан скандалах с индийскими и китайскими производителями – быть откровенным браком из-за несоблюдения банальной гигиены в цехах.
Неудивительно, что европейское сообщество, так сильно обжегшееся на халтуре индийских производителей в 2003–2017 годах, не рвется доверять индийскому заводу сейчас, когда от малейших колебаний качества вакцины зависит, будешь ли ты подключен к ИВЛ или нет. В случае с АстраЗенекой проблема осложняется и тем, что вакцина Oxford-AstraZeneca AZD1222 – рекомбинантная векторная, то есть относится не просто к лекарственным средствам, а к биофармацевтикам, средствам, полученным с помощью современных биотехнологий, генерик к которым (биосимиляр, биоаналог) не может быть стопроцентной копией оригинала по умолчанию4.
Covishield и Oxford-AstraZeneca AZD1222
А теперь, вооруженные этими данными, посмотрим на Ковишилд и АстраЗенека поближе.
Serum Institute of India (SII, Индийский институт вакцин) – довольно старое предприятие с международными связями. AstraZeneca уже работала с ним раньше, отдавая Институту заказы на производство своих вакцин для Бразилии, Южной Африки и Саудовской Аравии. Сейчас Институт массово производит вакцину АстраЗенеки, назвав ее Covishield (Ковишилд), для десятков стран с низким и средним уровнем дохода, а UK’s Medicines and Healthcare products Regulatory Agency (MHRA), фармрегулятор Великобритании, проводит в нем аудит, чтобы авторизировать Ковишилд для продажи и использования на территории самого Соединенного Королевства. Если MHRA авторизует вакцину, это откроет ей доступ и в страны ЕС, так как фармрегулятор Европейского Союза может согласиться с проверкой своего британского «коллеги» без дополнительных исследований.
Так чем же является Ковишилд – генериком или формой использования чужих производственных мощностей для производства своего препарата?
АстраЗенека говорит, что дала Институту Вакцин лицензию – то есть это уже выпадающий из определения традиционного генерика факт.
Далее, состав. Посмотрим на официальные сайты:
COVISHIELD, COVID-19 Vaccine (ChAdOx1-S [recombinant]), 5 mL solution for intramuscular injection, multiple dose vials. Each vial contains 10 doses (each dose is 0.5 mL)5.
ChAdOx1-S nCoV- 19 Corona Virus Vaccine (Recombinant) 5 × 10viral particles, 0.5 ml6.
Действующее вещество, количество – одинаковы. То есть формально первое условие идентичности оригинала и генерика – соблюдено.
Технология изготовления, судя по заявлениям АстраЗенеки и представителей Великобритании, тоже Индийскому институту вакцин предоставлена.
Каковы же наиболее интересующие нас биоэквивалентность, безопасность и эффективность?
Так как Ковишилд воспринимается как генерик – хотя и в довольно странном свете, – согласно мировой практике, Институт имеет право проводить исследования по Ковишилду в «обрезанном» варианте, потому что они уже были проведены для оригинальной Oxford-AstraZeneca AZD1222. Central Drugs Standard Control Organization (CDSCO, индийский фармрегулятор) утверждает, что для получения разрешение на экстренное применение вакцины (как в нашем случае) должны быть предоставлены данные о безопасности, эффективности и иммуногенности (способность вырабатывать антитела).
Есть ли такое исследование?
Есть исследование, которое сравнивает безопасность и иммуногенность у Ковишилда и оригинальной Oxford-AstraZeneca AZD1222. Заметьте – только вырабатывать антитела, не касаясь вопроса, будут ли они действовать эффективно.
Это рандомизированное, контролированное, полуослепленное исследование «гибридной» II–III фазы, которое сравнивает безопасность (на 1600 участниках, что мало для полноценной III фазы клинических исследований) и иммуногенность (на 400 участниках, что еще меньше от необходимого). Фактически это означает, что 1200 человек из исследования получали пустышку-плацебо, и только на 400 участниках (300 – Ковишилд, 100 – АстраЗенека) действительно сравнивали вакцины друг с другом7.
Это исследование является основой для утверждения про эквивалентность вакцин. Обратите внимание, здесь Институт выкладывает информацию об эффективности и безопасности по данным зарубежных исследований8.
И хотя отечественных данных по эффективности нет, CDSCO выдает разрешение на экстренное применение Ковишилду 3 января 2021 года.
ВОЗ также одобряет Ковишилд и вносит ее в мировой проект вакцинации COVAX, то есть считает ее эффективной и безопасной настолько, чтобы в сложившихся экстренных условиях рекомендовать9.
Канадский фармрегулятор также дает разрешение на употребление и продажу Ковишилда10.
Вакцинироваться Ковишилдом или нет?
Безусловно, учитывая прошлые «заслуги», нельзя не относиться без внимания к опасениям насчет индийских производителей, однако существует еще несколько факторов, влияющих на текущую ситуацию:
- Образование новых штаммов. Чем дольше затянется эпидемия, тем больше вероятность, что нынешние вакцины ничего не смогут поделать против новых штаммов.
- Безопасная технология самой вакцины – и Ковишилд, и АстраЗенека от вируса nCoV- 19 имеют только вирусный белок, он не способен навредить вакцинируемому.
- Шансы получить «нормальную» вакцину в ближайший год крайне низки.
Примечания
- 1. Мелинда Симмонс
- 2. Exclusive: UK auditing Indian vaccine site amid scramble for shots – sources
- 3. Mumbai: Eight doctors reject Serum Institute’s Covishield
- 4. Guideline on Similar Biological Medicinal Products Containing Biotechnology-derived Proteins as Drug Substance – Non Clinical and Clinical Issues
- 5. Serum Institute of India Pvt. Ltd.
- 6. Summary of the Public Assessment Report for AstraZeneca COVID-19 vaccine
- 7. A Phase 2/3, Observer-Blind, Randomized, Controlled Study to Determine the Safety and Immunogenicity of Covishield (COVID-19 Vaccine) in Healthy Indian Adults
- 8. 130th SEC COVID-19 Recommendations dated 09.12.2020
- 9. WHO lists two additional COVID-19 vaccines for emergency use and COVAX roll-out
- 10. Authorization of COVISHIELD with English-only Vial and Carton Labels




Комментарии