Девятый вал реакции воспаления, или Что такое цитокиновый шторм
Часть первая: Цитокины
Цитокиновый шторм – слово, с которым мы познакомились в начале 2000-х, когда вспыхнула эпидемия птичьего гриппа H5N1, хотя само явление чрезмерного или неконтролируемого выброса провоспалительных веществ организмом было знакомо специалистам гораздо раньше. Цитокиновый шторм наблюдается не только при инфекционных заболеваниях – но именно при вирусных инфекциях его изучили наиболее полно. В этой статье мы тоже присмотримся к нему поближе большей частью на примере «эталонной» для этого явления инфекции – гриппа.
Приход бури
Термин «цитокиновый шторм», описывающий нарушения в иммунной системе и неконтролируемую воспалительную реакцию, часто используется как в научной литературе, так и средствами массовой информации. Однако, хотя общая концепция избыточного или неконтролируемого высвобождения особых провоспалительных соединений-цитокинов хорошо известна, фактическое определение того, что представляет собой цитокиновый шторм, отсутствует. Кроме того, нет у ученых и ясного понимания о том, что ускоряет цитокиновый шторм на молекулярном уровне, о вкладе такого «шторма» в развитие болезни или о том, какие терапевтические стратегии могут быть использованы для его предотвращения или подавления.
Первое использование термина «цитокиновый шторм» принято связывать со статьей 1993 года, посвященной проблеме отторжения трансплантата, так называемой реакции «трансплантат против хозяина».
Использование же его в исследованиях, касающихся инфекционных заболеваний, началось в начале 2000-х. Цитокиновый шторм наблюдали при цитомегаловирусных инфекциях, заболеваниях, вызванных вирусом Эпштейна – Барр, стрептококком группы А, вирусом гриппа, вирусом натуральной оспы, а также при тяжелом остром респираторном синдроме (SARS), который был связан с коронавирусом SARS-CoV.
«Популярность» же цитокиновому шторму создала статья о птичьем гриппе H5N1 в 2005 году, после чего этот термин стал чаще появляться как в научной литературе, так и в публикациях СМИ.
Сейчас обычный поиск в Гугл словосочетания «Cytokine Storm» дает более четырех миллионов результатов (русскоязычный – только 20 000) – что говорит о том, что к моменту прихода COVID-19 широкие слои англоговорящего населения уже приблизительно понимали терминологию, в которой описывались опасности новой болезни.
Помимо собственно инфекционных заболеваний, неконтролируемая воспалительная реакция играет важную роль в реакции отторжения трансплантата, рассеянном склерозе, панкреатите или при синдроме полиорганной недостаточности. Цитокиновый шторм может возникнуть в ответ даже на неудачно подобранное терапевтическое лечение.
Волна и частицы
«Волны» цитокинового шторма обусловлены выбросом своеобразных частиц, которые объединяют общим словом «цитокины».
Цитокины представляют собой разнообразную группу небольших по размеру белков, которые секретируются клетками для того, чтобы передавать сигналы и коммуницировать друг с другом. Цитокины связываются с рецепторами и вызывают ответ в клетке-мишени – она начинает исполнять какую-то специфическую функцию: так, например, цитокины осуществляют контроль размножения и приобретения клетками специфических свойств, регулируют образование новых кровеносных сосудов и участвуют в иммунных и воспалительных реакциях.
Если упрощать все до максимума, то цитокин – это некий мячик, которым одна клетка бросает в другую, чтобы вызвать нужную реакцию. Все мячики разные, на каждый мячик возникает достаточно специфичная реакция, но, в то же время, так мячики – это мячики, то, помимо специфической, возникает еще и ряд реакций просто на мячик, общих для всех.
Наиболее известные цитокины – это интерфероны, интерлейкины, хемокины, колониестимулирующие факторы и фактор некроза опухолей.
Интерфероны регулируют врожденный иммунитет, активируют противовирусную защиту, тормозят развитие и возникновение раковых клеток (антипролиферативный эффект).
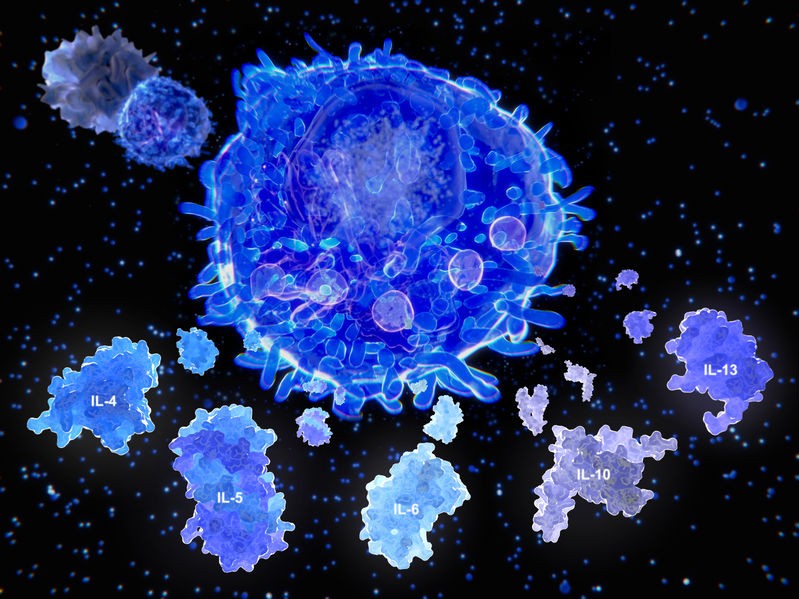
Интерлейкины «занимаются» ростом и дифференцировкой лейкоцитов; многие из них обладают провоспалительными, то есть «раздувающими» воспаление, свойствами.
Хемокины занимаются контролем хемотаксиса (способностью двигаться к раздражающим субстанциям: так, бактерии могут двигаться к еде и от токсических для них веществ), «рекрутированием» лейкоцитов; многие их них также провоспалительные.
Колониестимулирующие факторы стимулируют размножение и «дозревание» так называемых клеток-предшественников.
Фактор некроза опухолей активирует цитотоксические Т-лимфоциты.
Многие цитокины имеют по нескольку функций, которые иногда не связаны между собой, зависящие от клетки-мишени или от наличия или отсутствия других цитокинов. Некоторые задействуют разные рецепторы, но передают сигналы через обычные внутриклеточные пути (например, интерфероны типа I и типа III). Частично из-за этого разнообразия структуры и функции классификация и номенклатура цитокинов, а также оценка их участия в том или ином заболевании – не самое простое дело.
Так, хотя многие инфекции характеризуются очень похожим по количеству и составу цитокиновым ответом, их клинические проявления могут быть совершенно разными. Именно эта особенность, кстати, и играет при текущей пандемии COVID-19 одну из главных ролей – при всем понимании общего процесса цитокинового шторма медики не могут найти пути подавления его при этом конкретном заболевании, так как все предыдущие подходы оказались малоэффективными.
Рассмотрим же поближе цитокины, связанные с цитокиновым штормом.
Интерфероны
Интерфероны – это семейство цитокинов, которое в основном занимается процессами врожденного иммунитета к микробам и вирусамnih.gov.
Их принято классифицировать на основе их рецепторной специфичности на три основных типа – I, II и III. Наиболее известные из них интерфероны типа I (IFN-α и IFN-β) передают сигналы через гетеродимерный (то есть образованный двумя разными макромолекулами) рецепторный комплекс IFNAR1 / IFNAR2, а интерфероны типа II(интерфероны-γ) – через IFN-γR1 / IFN-γR2.
Лямбда-интерфероны представляют собой новый класс интерферонов с антивирусными свойствами. Они могут, например, защищать мышей от вируса гриппа А.
Интерфероны λ1, λ2 и λ3 (их также называют интерлейкинами – IL-29, IL-28a и IL-28b соответственно) связываются с рецепторным комплексом IL-28R / IL-10Rβ, но функционально сходны с интерферонами типа I, потому что передают сигналы по тому же сигнальному пути, что и интерфероны типа I (на этом примере уже можно убедиться, как тяжело классифицировать цитокины).
Связывание с рецепторами приводит к тому, что активируется целый ряд каскадных реакций, в результате которых включаются в работу сотни зависящих от стимуляции интерферонами генов. Эти гены кодируют белки с противовирусными, антипролиферативными или иммуномодулирующими свойствами. Такие особенности интерферонов привели к тому, что их используют в терапевтической практике (часто в сочетании с другими лекарственными средствами) при лечении вирусных заболеваний наподобие гепатитов C и B, некоторых типов лейкемии и лимфомы, а также рассеянного склероза (Friedman RM. 2008. Clinical uses of interferons).
Интерлейкины
В отличие от интерферонов, интерлейкины представляют собой семейство, которое регулирует иммунную систему. Они занимаются главным образом дифференцировкой (то есть приобретением специфических свойств) и активацией иммунных клеток. Интерлейкины могут быть как провоспалительными, так и противовоспалительными и, как и все цитокины, вызывают самые разнообразные реакции.
Сначала термин «интерлейкин» употреблялся для обозначения цитокинов, которые продуцируются лейкоцитами, участвующими в межклеточной коммуникации, однако в настоящее время известно, что интерлейкины могут продуцироваться различными типами клеток.
Номенклатура интерлейкинов, пожалуй, самая запутанная.
Так, как мы уже видели выше, часть интерферонов может называться интерлейкинами, а интерлейкин-1 (IL-1) на самом деле представляет собой семейство цитокинов, кодируемых 11 генами. Из-за того, что у некоторых членов семейства IL-1 обнаружились новые функции, в 2010 году номенклатура группы даже была пересмотрена.
IL-1α и IL-1β представляют собой провоспалительные цитокины, которые опосредуют ответ хозяина на инфекцию через прямые и косвенные механизмы. Так, они усиливают передачу сигналов острой фазы, доставку иммунных клеток к месту первичной инфекции, активацию эпителиальных клеток и вторичную продукцию цитокинов.
Еще один термин, тесно связанный с интерлейкинами (в частности, интерлейкинами-1), это инфламмасомы – макромолекулярные комплексы, отвечающие за активацию воспалительного ответа. Эти комплексы продуцируют IL-1β и IL-18, а их активность регулируется интерферонами типа I.
Так называемая реакция острой фазы, возникающая в ответ на инфекцию, приводит к огромному количеству разнообразных местных событий и системных перестроек и сопровождается в основном провоспалительными изменениями типа увеличения выработки специфических цитокинов, которые могут быть связаны с попыткой организма быстро избавиться от вируса.
Изменения, которые производят интерлейкины, иногда очень неоднозначны и требуют дальнейшего изучения. Так, с одной стороны, IL-1 опосредует острое иммунное повреждение легких, но, в то же время, в эксперименте увеличивает выживаемость мышей, инфицированных вирусом гриппа, за счет усиления ответов антител класса IgM и привлечения лейкоцитов CD4 + к месту инфекции.
Хемокины
Самое большое семейство цитокинов – это хемокины, их насчитывается около 50 штук, и это число постоянно увеличивается. Название «хемокины» происходит от способности этих соединений заставлять химически («хемо») двигаться («кины», кинезис) другие клетки. Хемокины действуют как хемоаттрактанты, контролируя миграцию клеток, главным образом иммунной системы, и участвуют в таких разнообразных процессах, как эмбриогенез, развитие и функционирование врожденного и приобретенного иммунитета, а также метастазирование рака (Raman D, Sobolik-Delmaire T, Richmond A. 2011. Chemokines in health and disease).
Отличительная особенность хемокинов, из-за которой их и выделяют в отдельную группу – взаимодействие с одним или несколькими рецепторами, связанными с особыми передающими G-белками.
Все хемокины, в зависимости от химического строения, подразделяются на четыре типа – CXC, CC, C и CX3C.
Большинство хемокинов усиливают воспаление и высвобождаются клетками в ответ на вирусную или микробную инфекцию. Высвобождение таких провоспалительных хемокинов приводит к привлечению клеток иммунной системы (нейтрофилов, моноцитов/макрофагов и лимфоцитов) к месту инфекции. При этом, несмотря на то, что большинство цитокинов обычно вызывают не только один, а сразу массу самых разнообразных эффектов, такой химический «призыв» хемокинами иммунных клеток может быть очень высокоспецифичным.
Например, CXCL8 (еще называемый IL-8), CCL2 (который также имеет другое название, MCP-1, то есть фактор хемотаксиса моноцитов-1) и CCL11 (эотаксин) притягивают соответственно нейтрофилы, моноциты и эозинофилы.
Использование хемокинов и их рецепторов давно является вожделенной целью для фарминдустрии – но пока без особого успеха.
Колониестимулирующие факторы
Колониестимулирующие факторы, как уже можно понять из названия, стимулируют клетки. Под их воздействием клетки – а мы сейчас говорим о клетках-предшественниках, незрелых, оставшихся еще с зародышевого периода клетках, присутствующих в нашем организме как своеобразные «строительные материалы», – из которых потом получаются уже известные нам лимфоциты, макрофаги, моноциты, эритроциты и множество других «конечных» клеток, начинают «дозревать» и приобретать специфические функции.
В случае иммунной системы это, например, гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), макрофагальный колониестимулирующий фактор (M-CSF) и гранулоцитарный колониестимулирующий фактор (G-CSF), относящиеся к общей ветке клеток крови.
Колониестимулирующие факторы, как и хемокины, тоже связаны с воспалением, и есть доказательства того, что эти факторы могут быть частью провоспалительной цитокиновой сети, которая включает в себя IL-1 и фактор некроза опухоли TNF.
Считается, что способствуя увеличению числа цитокинпродуцирующих макрофагов в месте воспаления, колониестимулирующие факторы могут быть частью каскадных реакций, приводящих к тому, что воспалительная реакция усиливается и хронизируется.
Фактор(ы) некроза опухоли
Фактор некроза опухоли TNF является, пожалуй, самым известным и наиболее активно изучаемым провоспалительным цитокином, и роль его в цитокиновом шторме весьма велика.
Название «фактор некроза опухоли» впервые был применено в 1975 году для определения цитотоксического сывороточного фактора, способного вызывать обратное развитие опухолей у мышей.
Вскоре после этого выяснилось, что он участвует также в патогенезе малярии и сепсиса.
В настоящее время фактор некроза опухоли считается основным цитокином, участвующим в иммунном ответе на острые вирусные заболевания, в том числе на грипп, лихорадку денге и лихорадку Эбола. Этот цитокин экспрессируется различными иммунными клетками, а его первичный рецептор TNFR1, по-видимому, экспрессируется вообще всеми типами клеток, из-за чего действие фактора некроза опухоли распространяется очень широко.
Фактор некроза опухоли – это не один белок, а целое семейство соединений, из них собственно TNF называют TNF-α.
Избыточная продукция фактора некроза опухоли связана с рядом хронических воспалительных и аутоиммунных заболеваний, поэтому лекарства из группы ингибиторов TNF успешно применяются при лечении воспалительных заболеваний кишечника, псориаза и ревматоидного артрита.
А вот в лечении сепсиса фактор некроза опухолей оказался бесполезен. Ученые связывают это с ранним высвобождением и коротким периодом полувыведения этого цитокина.
Итак, мы познакомились со всеми главными «действующими лицами» цитокинового шторма. О том, как они взаимодействуют и что медицина может противопоставить этому явлению, читайте в продолжении статьи.