Бактериофаги – старое имя новой технологии
История бактериофагов имеет множество точек отсчета.
Можно начать ее с Луи Пастера, который не смог выделить возбудителя бешенства при помощи сильнейшего на тот момент микроскопа и задумался (а, главное, заставил задуматься своих учеников, в число которых тогда входили ученые почти всех стран мира, приезжавшие к нему стажироваться) о природе болезнетворного агента.
Можно начать ее с Шарля Шамберлана, соратника Пастера, задавшегося сделать такой фильтр, который смог бы убирать из раствора бактерии, и тем выяснить, есть ли более малые формы патогенов, – и сделавшего его.
Можно вспомнить Адольфа Майера, который изучал то, что мы теперь называем «вирус табачной мозаики», и путем сложной фильтрации избавил раствор от бактерий, но так и не нашел возбудителя – зато смог сподвигнуть на продолжение своих экспериментов Дмитрия Ивановского и Мартина Бейеринка, первый из которых все же доказал, что в фильтрате остается нечто, что продолжает заражать листья табака (но ошибочно решил, что это токсины), а второй предположил, что это особый, новый вид возбудителя, и, собственно, первым сказал слово «вирус».
«Contagium vivum fluidum» – заразная живая жидкость, так Мартин Бейеринк описал болезнетворный агент табачной мозаики1.
А можно вспомнить чудеснейших Нобелевских лауреатов – немецкого физика Эрнста Руску, «отца» электронного микроскопа, и американского биохимика Уэнделла Мередита Стэнли, при помощи этого микроскопа в 1935 году впервые визуализировавшего и показавшего миру то, чье существование до него научное сообщество могло доказать лишь косвенно – сам вирус.
Однако мы начнем ее с Феликса Д’Эрелля.
Остап Бендер от микробиологии
Феликс Д’Эрелль был невероятным авантюристом. Самоучка, «несколько месяцев посещавший лекции в Боннском университете»2, в конце девятнадцатого века он уехал в Канаду на заработки, где пытался заниматься одновременно алкогольным производством, шоколадной фабрикой и кустарной микробиологией. Фабрика прогорела, написанная научная статья про углерод оказалась провальной в основе (Д’Эрелль считал, что углерод – это соединение, а не элемент), деньги закончились, и молодой человек, на досуге почитывавший труды Пастера, поскольку тот описывал интересующее Д’Эрелля брожение, успешно «продал» себя правительству Гватемалы в качестве... бактериолога. И в качестве бактериолога же начал самопально производить вакцины от малярии и желтой лихорадки. А параллельно – гнать виски из бананов.
Так наш герой впервые стал на путь, который в итоге приведет его к бактериофагам, которыми он сможет заинтересовать весь мир: работа с ферментацией даст денег и возможность вернуться к микробиологии, микробиология – экспериментировать с микроорганизмами и их применением.

Феликс Д’Эрелль
Источник: wikipedia.org.
В 1915 году уже имевшему опыт работы с бактериями и медикаментами Д’Эреллю (до войны он, бросив и «медицинскую» латиноамериканскую карьеру, и алкогольный бизнес, пристроился волонтером в Пастеровский институт и пытался бороться с саранчой при помощи коккобацилл, а во время войны занимался производством медикаментов для армии) на глаза попались труды английского бактериолога Фредерика Туорта, который обнаружил некий агент, могущий заражать и убивать бактерии, но не придал этому особого значения. Д’Эрелль значение придал – и через два года объявил об открытии «невидимого антагонистического микроба дизентерийной палочки», бактериофага.
Выделял он его так (и это в дальнейшем будет использоваться всеми его последователями, включая советских ученых):
- Питательная среда заражается бактериями – среда становится непрозрачной.
- Бактерии заражаются фагами и погибают, производя новые фаги – среда становится прозрачной.
- Среда фильтруется через керамический фильтр, который задерживает бактерии и крупные объекты – в фильтрате оказываются лишь фаги.
В начале 1919 года Д’Эрелль успешно провел эксперименты на курах и тут же начал применять свое «инновационное лечение» на людях.
В то время никто, включая его главного разработчика, точно не знал, что такое бактериофаг. Кто-то, как и Д’Эрелль, считал, что это живой организм, который размножается, питаясь бактериями. Кто-то – что это просто вещество, возможно фермент, который находится в бактериях и запускает высвобождение неких белков, из-за чего бактерия гибнет. Из-за того, что Д’Эрелль ничтоже сумяшеся звонил на каждом углу (а Д’Эрелль отличался редкостным талантом к саморекламе, что и позволяло ему успешно осуществлять все свои авантюры) о «прорыве в медицине» и «стопроцентном излечении от болезни», не проведя достаточного количества исследований и не выяснив даже, что именно вызывает лизис бактерий, его постоянно критиковали другие, «настоящие» ученые. Самоучка, работающий на общественных началах лаборантом и на том основании причисляющий себя к людям науки, стоял им как кость в горле.
Именно эта скандальность и дилетантство и послужили причиной изгнания Д’Эрелля из альма матер – вернувшись из Индокитая, где он боролся с эпидемиями, «отец фаготерапии» внезапно обнаружил, что возвращаться ему по сути некуда – за время его отсутствия замдиректора Пастеровского института, с которым наш герой имел постоянные трения, лишил «безоплатного лаборанта» доступа в лабораторию и запретил его исследования.
Но Д’Эрелля этим было не остановить – он собрал свои вещи и «съехал» в лабораторию к знакомому биологу, где продолжил эксперименты и уже через год – обманом и под видом официальной институтской публикации – выпустил в печать свою монографию по фагам, полностью уверенный в собственной правоте и в успехе своего открытия.
И успех пришел.
Признания и награды посыпались на Д’Эрелля как из ведра: в 1924 году он получил почетную докторскую степень Лейденского университета и медаль Левенгука, в следующем году – номинировался на Нобелевскую премию, Великобритания наняла его для борьбы с холерой и чумой в Индии, США пригласили преподавать в Йеле, множество фирм в Европе и Америке одна вперед другой бросились производить бактериофаги...
Однако популярность вскрыла и недостатки незавершенности исследований и неотработанности технологии – при массовом производстве оказалось, что фаги совсем не так эффективны, как это обещал их первооткрыватель. Научное сообщество (которое Д’Эрелль все эти годы настраивал против себя) отвернулось от него, бизнес начал чахнуть.
Д’Эрелль попытался возродить свою славу еще дважды: первый раз – переехав в Грузию по приглашению своего коллеги, бывшего «пастеровца» Георгия Элиавы, который был влюблен в идеи фаготерапии еще с 20-тых (откуда у СССР и оказалась технология производства фагов), а второй – когда, сбежав из Грузии после расстрела все того же Элиавы как врага народа, внезапно обнаружил, что на родине военные успешно продвигают его открытие.

Д’Эрелль и Георгий Элиава в 1918 году
Источник: burusi.wordpress.com.
Впрочем, европейский триумф закончился еще быстрее советского – сначала немцы оккупировали Францию и Д’Эрелль оказался под домашним арестом, а потом в медицинскую практику ворвались антибиотики...
Д’Эрелль умер вскоре после войны в безвестности, но труды его не пропали даром – Макс Дельбрюк, Нобелевский лауреат, физик и генетик, используя Д’Эреллевские бактериофаги, открыл механизм реплицирования и генетическую структуру вирусов, создав по сути такое направление в науке, как молекулярная биология; медики СССР, не имея доступа к нормальным антибиотикам (советский пенициллин-крустозин ВИЭМ содержал в себе, увы, лишь 10% действующего вещества, а все остальное представляли более или менее токсичные примеси)3, активно использовали фаги как на полях Второй мировой, так и после нее; благодарные парижане назвали его именем проспект... До двухтысячных казалось, что этим наследие Д’Эрелля и исчерпывается.
Однако в начале нового века растущая проблема антибиотикорезистентности заставила ученых уже под новым углом и с новыми методиками посмотреть в сторону давно забытого старого.
В 1994 году Soothill исследовал эффективность бактериофагов для борьбы с синегнойной палочкой, которая нередко вызывает инфекционный процесс при трансплантациях лоскутов кожи, и пришел к выводу, что они могут быть полезны4. С тех пор обзоры, касающиеся лечения бактериофагами, появляются на базе данных PubMed почти каждый месяц. Согласно данным платформы Web of Science, в последние годы среднее число их цитирований за год составляло около 1100, а в 2017 году увеличилось до 1400.
Так эффективна или не эффективна на самом деле методика авантюриста Д’Эрелля и как ее видит современная наука?
Другой подход к борьбе с бактериями
Начнем с того, что бактериофаги действительно существуют. Более того – они являются одним (если не самым) распространенным биологически объектом на Земле: в мире существует приблизительно 10 31 до 10 32 фагов (так сокращают слово «бактериофаги» в западной медицинской литературе). Сейчас термином «бактериофаги» принято обозначать вирусы, поражающие бактерии и играющие ключевую роль в ограничении их популяции. Это естественные враги бактерий, их можно найти в почве, сточных водах, воде и других местах, где обитают последние. Именно они, например, ответственны за гибель приблизительно 20-40% всех морских поверхностных бактерий каждые 24 часа5.
Современное лечение болезней при помощи бактериофагов на Западе называют Phage Therapy (фаготерапия). Она до сих пор не очень распространена – и не в последнюю очередь потому, что исследование бактериофагов все еще продолжается. На данный момент для уничтожения бактерий используются около 19 семейств фагов, большая часть которых представлена ДНК-вирусами.
Также современное общество использует фаги в ветеринарии и сельском хозяйстве. Если объектом, в котором действуют фаги, является не человек или животное, то употребляется термин «биоконтроль»6.
Классификация бактериофагов согласно Международному комитету по таксономии вирусов
|
Порядок |
Семейство |
Нуклеиновая кислота |
|
Сaudovirales |
Myoviridae |
ДНК |
|
Siphoviridae |
ДНК |
|
|
Podoviridae |
ДНК |
|
|
Ligamenvirales |
Lipothrixviridae |
ДНК |
|
Rudiviridae |
ДНК |
|
|
Неизвестен |
Ampullaviridae |
ДНК |
|
Bicaudaviridae |
ДНК |
|
|
Clavaviridae |
ДНК |
|
|
Corticoviridae |
ДНК |
|
|
Cystoviridae |
РНК |
|
|
Fuselloviridae |
ДНК |
|
|
Globuloviridae |
ДНК |
|
|
Guttaviridae |
ДНК |
|
|
Inoviridae |
ДНК |
|
|
Leviviridae |
РНК |
|
|
Microviridae |
ДНК |
|
|
Plasmaviridae |
ДНК |
|
|
Tectiviridae |
ДНК |
Как работает фаготерапия
Бактериофаги уничтожают бактерии двумя путями: или встраивая себя в клетку бактерии и потом сразу же уничтожая ее при размножении (литический цикл), или удваиваясь при каждом делении клетки и достигая определенного количества перед тем, как уничтожить бактерию (лизогенный цикл), причем во втором случает фаг может сделать до 1000 копий себя в каждой бактерии, а потом освободить их все разом.
Большинство фагов обычно может менять один цикл на другой.
Бактериофаги могут размножаться и расти только внутри бактерии. Как только все бактерии лизируются (погибают), размножение фагов прекращается.
Также, как и другие вирусы, фаги могут находиться «в спячке», пока не появится достаточное количество бактерий.
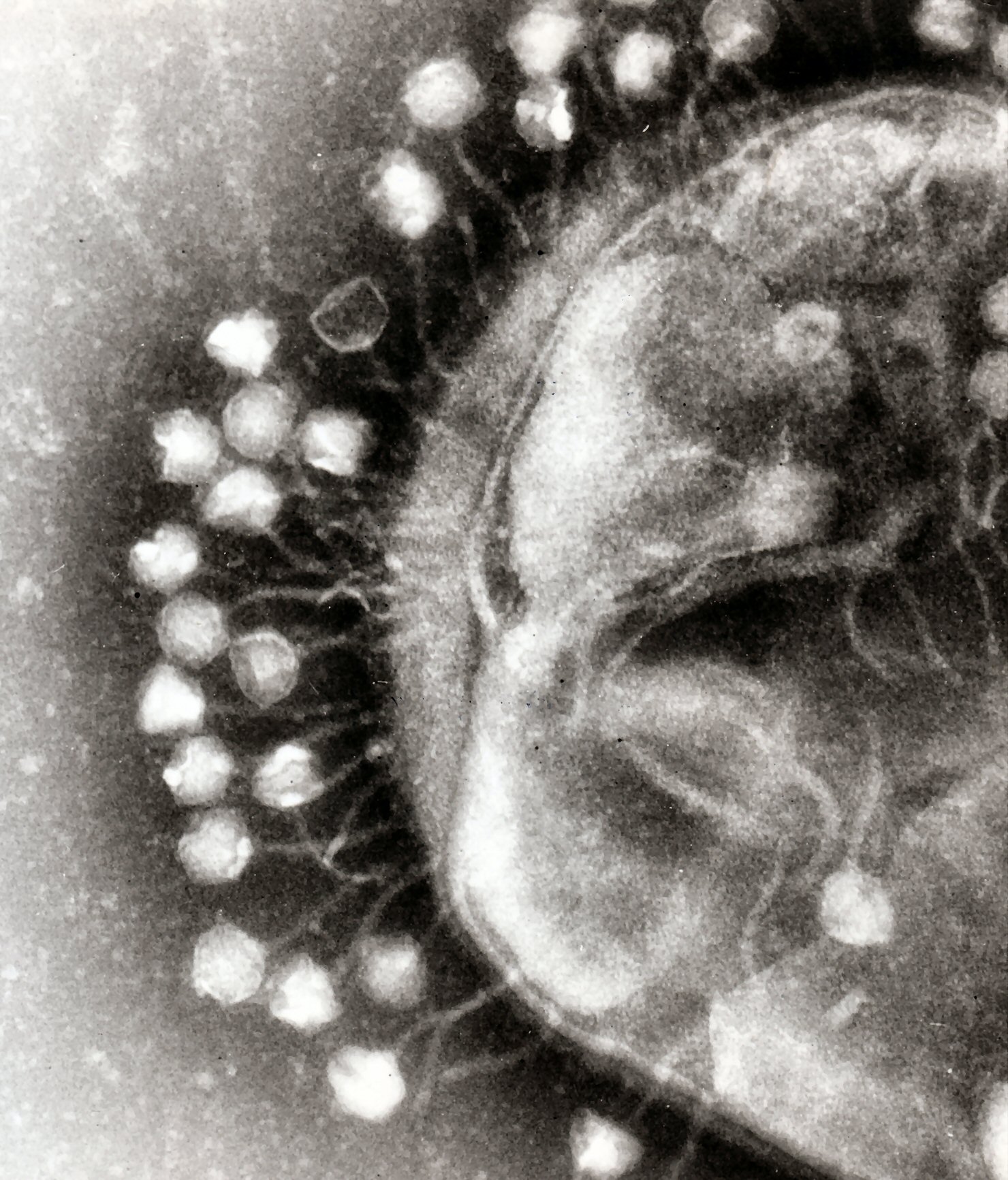
Бактериофаг. Источник: wikipedia.org.
Фаготерапия или антибиотикотерапия
Появление антибиотиков в середине 20-го века произвело революцию в здравоохранении и кардинально улучшило как качество, так и продолжительность жизни. Например, в 1900 году продолжительность жизни мужчин и женщин даже в такой промышленно развитой стране, как США, составляла 46 и 48 лет соответственно, а основными причинами смерти были инфекционные заболевания типа дифтерии, брюшного тифа, чумы, туберкулеза, сифилиса и так далее.
Антибиотики начали новую эру в медицине, быстро став незаменимыми: так, в тех же США в 2011 году выписывалось 842 рецепта на антибиотики на 1000 человек7.
Но с распространением антибиотикотерапии общество столкнулось с проблемой роста устойчивости бактерий к этим препаратам. На данный момент гены устойчивости к антибиотикам в изобилии присутствуют в окружающей среде, и многие антибиотики обладают снижающейся эффективностью в отношении распространенных инфекций, в частности, трудно поддающихся лечению нозокомиальных инфекций, вызываемых так называемой группой ESKAPE (Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa и Enterobacter spp.)8. Ситуация настолько угрожающая, что Центры по контролю за заболеваниями (CDC) и ВОЗ, например, объявили устойчивость к антибиотикам угрозой для глобального здравоохранения9.
Опасность состоит даже не в том, что бактерии вырабатывают устойчивость каждая для себя – опасность в том, что они способны «обучать» этой устойчивости другие бактерии своего и даже не своего вида. Поэтому при применении антибиотиков необходимо всегда помнить о следующих правилах:
- Пользуйтесь антибиотиками только при инфекциях бактериального происхождения. Антибиотики не лечат вирусные инфекции (ОРВИ, грипп, герпес и так далее).
- Не используйте антибиотики «профилактически».
- Принимайте антибиотики строго по назначенной схеме и придерживайтесь назначенной дозировки.
- Завершите курс антибиотиков, даже если вы почувствовали себя лучше.
- Не принимайте антибиотики с истекшим сроком годности.
- Выбрасывайте антибиотики с истекшим сроком годности или неиспользованные антибиотики.
- Не давите на своего врача, чтобы он назначил вам вашему ребенку антибиотики «на всякий случай».
Также с антибиотиками связана и другая проблема – они убивают не только патогенные, но и все остальные бактерии в нашем организме, а человеку для нормальных процессов пищеварения, производства витаминов и здоровой конкуренции с патогенными микроорганизмами нужны и «хорошие» бактерии. Именно с уничтожением полезной микрофлоры связаны такие побочные эффекты антибиотиков, как расстройство желудка, тошнота и рвота, вздутие живота и повышенное газообразование, понос, а также грибковые инфекции (наиболее «популярной» из которых является кандидоз).
И вот здесь, конечно, бактериофаги наиболее ярко демонстрируют свое преимущество.
Каждый вид фагов атакует только «свои», определенные бактерии, поэтому его можно использовать для более целенаправленного, точечного лечения. Уничтожая, например, стрептококк, вызывающий воспаление горла, бактериофаг не будет трогать лактобактерии в нашем кишечнике.
Кроме того, фаги показывают результаты не хуже антибиотикотерапии.
Вот, например, данные относительно свежего обзора 2017 года10
|
Возбудитель |
Модель |
Итог |
|
Shigella dysenteriae |
Человек |
Все четверо пациентов выздоровели через 24 часа |
|
Vibrio cholerae |
Человек |
68 из 73 выжили в группе лечения фаготерапией против 44 выживших из 118 человек контрольной группы |
|
Pseudomonas aeruginosa |
Мышь |
Снижение смертности на 66,7% |
|
Clostridium difficile |
Хомяк |
Пероральное совместное введение вместе с клостридией предотвратило развитие инфекции |
|
Хомяк |
Пероральный прием каждые 8 часов в течение 72 часов снизил смертность на 92% |
|
|
Устойчивый к ванкомицину Enterococcus faecium |
Мышь |
Снижение смертности на 100% |
|
Продуцирующая β-лактамазу Escherichia coli |
Мышь |
Снижение смертности на 100% |
|
Устойчивая к имипенему Pseudomonas aeruginosa |
Мышь |
Снижение смертности на 100% |
|
Acinetobacter baumannii, Pseudomonas aeruginosa и Staphylococcus aureus (сепсис) |
Мышь |
Введение фагов защитило животных от смертельной дозы A. baumannii и P. aeruginosa, но не от S. aureus |
Есть и данные успешного клинического применения фаготерапии. Так, например, врачи смогли вылечить при помощи бактериофагов 68-летнего мужчину из Калифорнии, который страдал инфекцией, вызванной Acinetobacter baumannii и до этого три месяца безуспешно лечился антибиотиками11.
Обзор 2011 года Pros and cons of phage therapy12 перечисляет основные плюсы фаготерапии:
- Фаги действуют как против чувствительных, так и против устойчивых к антибиотикам бактерий.
- Их можно использовать отдельно или вместе с антибиотиками и другими лекарственными средствами.
- Фаги размножаются и их количество увеличивается во время лечения (может потребоваться только одна доза).
- Они могут лишь незначительно влиять на «хорошие» бактерии в организме.
- Бактериофаги – естественный компонент окружающей среды, поэтому их легко обнаружить и выделить.
- Фаги не являются токсичными для человека, животных растений и окружающей среды.
Недостатки фаготерапии
Казалось бы, все перечисленное должно немедленно отвратить медицину от применения антибиотиков и перейти на использование бактериофагов.
Однако это не так. Фаготерапия на данный момент до конца не изучена и требует дополнительных исследований. Мы не можем, как Д’Эрелль, выпускать на рынок средство, не прошедшее все испытания.
Так, например, до сих пор неизвестно, могут ли бактериофаги вредить людям или животным способами, не связанными с прямой токсичностью. Кроме того, остается вопросом, может ли фаготерапия стать причиной того, что бактерии выработают устойчивость и к бактериофагам и станут сильнее их.
Минусы фаготерапии можно свести к следующим пунктам:
- Фаги в настоящее время трудно подготовить для использования людьми и животными.
- Неизвестно, какую дозу или количество фагов следует использовать.
- Неизвестно, сколько времени может занять фаготерапия.
- Найти специфичный для лечения инфекции бактериофаг иногда бывает весьма трудно.
- Фаги могут вызвать чрезмерную реакцию иммунной системы.
- Типов фагов может не хватить для лечения всех бактериальных инфекций.
- Некоторые фаги могут вызвать устойчивость бактерий.
Фаготерапия, несмотря на растущее число конгрессов и организаций, одобрительно относящихся к ее использованию (например, EMA, Европейское агентство лекарственных средств, в 2015 году провело конференцию, посвященную фагам, и пришло к выводу о целесообразности их использования), еще не одобрена для применения в качестве способа лечения людей в США и Западной Европе (кроме единственного отделения во Вроцлаве – еще одном центре, который в начале века перенял идеи Д’Эрелля)13. Одна из причин этого заключается в том, что антибиотики более доступны и считаются более безопасными в использовании. В настоящее время ведутся исследования наилучшего способа использования бактериофагов у людей и животных и доработка вопросов их безопасности.
Бактериофаги и пищепром
Однако, несмотря на сохраняющиеся вопросы к применению в качестве терапии, бактериофаги активно используются в пищевой промышленности. Так, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (U.S. Food and Drug Administration, FDA) одобрило применение некоторых фаговых коктейлей (смеси фагов, применяющейся, когда возбудитель точно не известен или подозреваются несколько возбудителей одновременно) для предотвращения роста бактерий в пищевых продуктах. Бактериофаги, используемые как биоконтроль (так, как уже упоминалось выше, называется использование бактериофагов в неживых объектах), не дают развиваться огромному количеству опасных бактерий, могущих вызвать пищевое отравление, в том числе и хорошо известным всем:
- сальмонелле,
- листерии,
- кишечной палочке,
- микобактериям туберкулеза,
- синегнойной палочке и
- Campylobacter.
С этой целью фаги добавляются в некоторые полуфабрикаты, колбасу, сыры, и тому подобное, что на Западе называют «processed foods».
Также сейчас активно рассматривается вопрос возможности добавления бактериофагов в чистящие средства для уничтожения бактерий на поверхностях. Это может помочь поддержать стерильный режим в больницах, бороться с распространением инфекций в ресторанах и других общественных местах.
Перспективы
Фаготерапии уже сто лет, и она прошла путь от «живой жидкости» до генотипирования вирусов и классификации их по семействам, однако применение бактериофагов в качестве способа лечения людей и животных все еще недостаточно изучено. Текущие исследования и ряд случаев успешного клинического применения дарят нам надежду, что бактериофаги имеют потенциал войти в арсенал медицины наравне с антибиотиками, и, поскольку их применение в пищевой промышленности уже считается безопасным и одобрено, это может произойти довольно скоро.
Но торопиться с выводами не следует. Поспешность загубила карьеру первооткрывателя фаготерапии Д’Эрелля и отсрочила масштабное изучение бактериофагов более чем на 50 лет, поэтому повторная ошибка здесь недопустима.
Примечания
- 1. Мартин Бейеринк
- 2. Summers WC. Félix d'Hérelle and the Origins of Molecular Biology
- 3. Наталья Зейфман, Галина Зыкова. Из истории пенициллина в СССР после войны
- 4. Bacteriophage prevents destruction of skin grafts by Pseudomonas aeruginosa
- 5. Suttle CA. Marine viruses--major players in the global ecosystem
- 6. Phage therapy: An alternative to antibiotics in the age of multi-drug resistance. Derek M Lin, Britt Koskella, and Henry C Lin
- 7. US outpatient antibiotic prescribing variation according to geography, patient population, and provider specialty in 2011. Hicks LA и другие
- 8. Zhang XX, Zhang T, Fang HH. Antibiotic resistance genes in water environment
- 9. Centers for Disease Control. 2017. Antibiotic Resistance: The Global Threat
- 10. Phage therapy: An alternative to antibiotics in the age of multi-drug resistance. Derek M Lin, Britt Koskella, and Henry C Lin
- 11. Development and use of personalized bacteriophage-based therapeutic cocktails to treat a 2 patient with a disseminated resistant Acinetobacter baumannii infection
- 12. Catherine Loc-Carrillo and Stephen T Abedon
- 13. EMA