История мРНК вакцин – как возникала технология
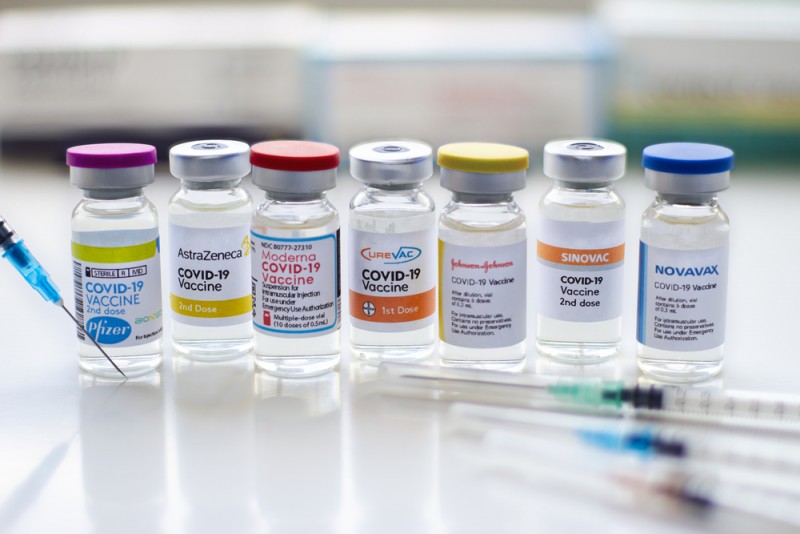
Один из самых частых аргументов противников вакцинации от COVID-19 – «как можно доверять только что придуманным вакцинам». Однако это не так. История мРНК вакцин, например, насчитывает... шестьдесят лет.
Статья опирается на обзор журнала Nature.
Первые
Да-да, вы не ошиблись: история мРНК-вакцин начинается в далеком 1961 году, когда Сиднеем Бреннером было описано наличие специфической молекулы, копирующей информацию с нашей ДНК (он со своей группой нашел ее еще в 1960-м, но пошел навстречу другим исследователям, не знавшим о его изысканиях и работавших над той же темой – в результате статьи двух коллективов вышли одновременно, потрясающий пример коллегиальности)1.
мРНК (информационная, матричная РНК) синтезируется на основе ДНК и содержит всю информацию о кодированных белках. Ее задача – считать информацию с ДНК и передать ее рибосомам, которые по этой «инструкции» произведут соответствующие белки. После того, как информация передана, мРНК разрушается. Длительность ее жизни – от нескольких секунд до нескольких дней, в зависимости от модификации.
Однако мРНК – это еще не лекарство на ее основе.
Вторая линейка открытий, связанных с мРНК-вакцинами, стартует чуть позже, в 1965-м, когда были открыты липосомы – базовая «система доставки» мРНК в клетку-мишень. И началось.
В 1969 – мРНК транслирована в лаборатории, 1971 – липосомы приспособлены для транспортировки лекарств, 1974 – липосомы использованы для доставки вакцины, 1978 – мРНК при помощи липосом доставлена в клетку... Но почему же мы не получили мРНК вакцины еще в 80-тых, спросит внимательный читатель. Ответ будет странным для нас теперешних – ученые не верили в пользу и прибыльность своего открытия!
Итак, 1978 год. Открытые семь лет назад липосомы используют для транспортировки генетического материала в клетки мыши2 и человека, чтобы вызвать экспрессию белка3.
Липосомы служат своеобразным контейнером для перевозки и, одновременно, защитой для мРНК, а дойдя до цели, сливаются с клеточными мембранами и «сбрасывают» свое содержимое в клетки. Защита мРНК очень нужна, ведь в нашем организме всегда присутствуют специфические ферменты РНКазы, которые ее разрушают. Капсула же из липосомы не дает ферментам «увидеть» свою цель.
Однако в то время мало кто видел в мРНК лекарственное средство – ведь в 70-е еще не было возможности производить генетический материал в лаборатории. Эксперименты преследовали цель исследования основных молекулярных процессов. мРНК выделяли обычно из крови кролика или других лабораторных животных.
В 1984 году, когда биологи Криг, Мелтон, Маниатис и Грин из Гарварда создали мРНК в лаборатории при помощи фермента, взятого у вируса, положение дел впервые изменилось. Ученые ввели свою синтезированную мРНК в кладку лягушки и показали, что она работает так же, как и настоящая. Но и они все еще рассматривали синтетическую мРНК в основном как исследовательский инструмент для изучения функции и активности генов4.
РНК-технологии не считались тогда перспективными в плане получения прибыли. Гарвардская группа, синтезировавшая мРНК, даже не подумала патентовать свой метод. Они просто... отдали свои реагенты Promega Corporation – компании, которая занималась поставкой реагентов в лаборатории – за небольшой гонорар и ящик шампанского «Вдова Клико». Promega , в свою очередь, сделала инструменты синтеза РНК доступными для других ученых.
Непризнанные
А вот другой исследователь, Роберт Мэлоун, в конце 1987 года смешавший нити матричной РНК с липосомами и «искупавший» в полученной смеси человеческие клетки, которые поглотили мРНК и стали послушно воспроизводить белки по ее «инструкции», думал уже иначе5.

Роберт Мэлоун, посередине, фото с личного твиттера ученого
Его опыты стали первым яблоком раздора в саду открытий, связанных с мРНК. Понимая, что результаты эксперимента могут иметь большое влияние на развитие медицины и принести большую прибыль, Мэлоун, тогда аспирант Института биологических исследований Солка в Калифорнии, сделал несколько заметок, которые подписал и датировал. Так, в частности, он написал, что если бы клетки могли создавать белки согласно «инструкции» доставленной в них мРНК, можно было бы «рассматривать РНК как лекарство». После этого он повторно провел эксперимент – уже на лягушачьих эмбрионах, – и снова увидел, что ткани поглощают мРНК и воспроизводят закодированные белки. Это был первый случай использования липосом для облегчения проникновения мРНК в живой организм.
Однако его успехов никто особо не оценил. Более того, несмотря на успешное использование липосом для доставки мРНК в клетки человека и эмбрионы лягушки, Мэлоун так и не получил докторскую степень. Он поссорился со своим руководителем и в 1989 году бросил аспирантуру, чтобы работать на Филипа Фельгнера, биохимика, который в настоящее время возглавляет Центр исследований и разработок вакцин в Калифорнийском университете в Ирвине.
Компания Фельгнера называлась Vical. Мэлоун, воспользовавшись опытом гарвардской группы, тоже синтезировал мРНК для своих экспериментов, но добавил липосомы нового типа, несущие положительный заряд, что повысило способность материала взаимодействовать с отрицательно заряженным остовом мРНК. Эти липосомы были разработаны Фельгнером.
И тут начались проблемы. Дело в том, что над похожей проблемой работал и бывший научрук Мэлоуна, Верма. В марте 1989 года и Верма (от имени Университета Солка), и Vical (совместно с Университетом Висконсина) подали заявки на патенты. И хотя все вроде бы кончилось хорошо: Университет Солка отказался от своих требований, – Верма... присоединился к Vical.
Мэлоун утверждает, что Верма и Vical заключили тайную сделку, в результате которой интеллектуальная собственность перешла к Vical. Патент был оформлен таким образом, что Мэлоун, числившийся одним из группы изобретателей, больше не мог получать личную выгоду от последующих лицензионных сделок, равно как и от любых патентов, выданных Университетом Солка. Мэлоун разругался уже с Фельгнером и ушел из Vical.
Он закончил мединститут и даже год практиковал, прежде чем вернуться в науку, где отчаянно пытался продолжить исследования мРНК-вакцин, но так не смог выбить финансирование. (Звучит, как анекдот: в 1996 году он пытался доказать чиновникам штата Калифорния, что необходимо вложить деньги в разработку мРНК-вакцины для борьбы с сезонными коронавирусными инфекциями.)
Потерпев поражение, Мэлоун сосредоточился на ДНК-вакцинах и технологиях доставки, потом занялся коммерческой деятельностью и консалтингом. А в последние несколько месяцев занят тем, что жалуется, что его «вычеркнули из истории», требует Нобелевскую и публично критикует (видимо, из вредности, потому что его идеи уже неоднократно опровергались результатами исследований) безопасность мРНК-вакцин.
А гарвардская группа пошла другим путем. Мелтон в том же 1987 году обнаружил, что мРНК может использоваться как для активации, так и для прекращения процесса производства белка, и создал компанию под названием Oligogen (позже переименованную в Gilead Sciences – помните историю с заоблачными ценами на софосбувир, лекарство от гепатита?), где стал изучать способы использования синтетической РНК для блокировки экспрессии генов-мишеней с тем, чтобы лечить таким образом болезни. О вакцинах он и его коллеги не думали.
Десятилетие фальстартов
В 1991 году Vical Фельгнера заключил многомиллионный договор с американской фармкомпанией Merck, одним из крупнейших в мире разработчиков вакцин. Merck`у понравилась идея использования мРНК для новой противогриппозной вакцины... но очень быстро он от нее отказался, поскольку стоимость производства была очень высокой.
Маленькая биотехнологическая фирма Transgène из Франции столкнулись с похожей проблемой. В 1993 году группа ее исследователей под руководством Пьера Мёльена стала первой, кто показал, что мРНК, упакованная в липосомы, может вызывать специфический противовирусный иммунный ответ у мышей6.
Ученые запатентовали свое изобретение и продолжили работу над мРНК-вакцинами. Но Мёльен, который сейчас возглавляет Innovative Medicines Initiative, подсчитал, что ему нужно как минимум 100 миллионов евро для оптимизации платформы – и сознательно похоронил свою идею. Как он сейчас говорит: «Я не собирался просить денег у своего начальства на такое сомнительное, рискованное дело». Срок действия патента истек, когда фирма-владелец компании Transgène решила прекратить его поддерживать.
Группа Мёльена переключилась на разработку ДНК-вакцин и систем доставки на основе векторов. В наше время ДНК-вакцины используются в ветеринарии, но их применение у людей ограничивается совсем недавним, месячной давности, экстренным разрешением, которое выдал фармрегулятор Индии вакцине против COVID-19.
Почему разработки ДНК-вакцин важны и для РНК-вакцин? Потому что вместе с развитием технологии развивалась и отрасль вакцин на основе нуклеиновых кислот вообще. Многое их того, что узнали на опыте ДНК-вакцин (особенности производства, введения в клиническую практику, идеи по поводу используемых молекул и последовательностей), можно применить и к РНК.
Онкологический период
Все 90-е и большую часть нулевых почти все фармфирмы-производители вакцин, заинтересовавшиеся технологией мРНК, в итоге перенаправляли свои деньги в другие разработки, потому что мРНК слишком быстро распадалась, а производство ее было слишком дорого. Мэтт Винклер, который в 1989 году основал в Техасе одну из первых компаний, специализирующихся на поставках мРНК, Ambion, сейчас признается: «С мРНК было ужасно сложно работать. Если бы меня тогда спросили меня, можно ли кому-нибудь ввести мРНК в составе вакцины, я бы посмеялся».
Однако идея вакцины на основе мРНК снова всплыла – на этот раз в среде онкологов, которые видели в ней, правда, лекарственный препарат, а не средство для предотвращения болезни. Начиная с Дэвида Кьюриела, несколько ученых и фармакологических стартапов стали изучать, можно ли использовать мРНК для борьбы с раком. Считалось, что если мРНК будет кодировать раковые белки, то введение ее в организм может научить иммунную систему атаковать те клетки опухоли, которые в естественном состоянии она не видит.
В 1995 году Кьюриел, который сейчас работает в Университете Вашингтона (Сент-Луис), добился определенных успехов опытах на мышах7. Но когда он обратился к Ambion по поводу превращения результатов его экспериментов в препарат, компания сказала ему: «Эта технология совершенно финансово не выгодна».
К счастью, другой иммунолог, Эли Гилбоа, специализирующийся на онкологических заболеваниях, добился большего успеха, да такого, что в 1997 году была основана первая компания, специализирующаяся на мРНК как на лекарственном средстве. Эли Гилбоа предложил брать иммунные клетки из крови пациента и «убеждать» их считывать информацию с синтетической мРНК, кодирующей опухолевые белки. Затем клетки вводились обратно в тело, где направляли иммунную систему на атаку скрытых опухолей.
Гилбоа и его коллеги из Медицинского центра Университета Дьюка в Северной Каролине продемонстрировали это в экспериментах на мышах. К концу 1990-х годов начались испытания и на людях, и побочный коммерческий проект Гилбоа, Merix Bioscience (теперь носящий название CoImmune), тоже начал заниматься разработкой препарата.
Все выглядело многообещающим до тех пор, пока несколько лет назад вакцина-кандидат, пройдя все начальные стадии клинических испытаний, не провалилась на последних тестах. Сейчас такой подход к лечению уже во многом устарел.
Но работа Гилбоа не пропала даром. Его опыты вдохновили основателей немецких фирм CureVac и BioNTech – двух крупнейших компаний, выпускающих мРНК, – начать исследовать мРНК. И Ингмар Хёрр из CureVac, и Угур Шахин из BioNTech признавались, что, узнав о том, что у Гилбоа получилось, они захотели повторить его эксперименты – но уже непосредственно введя мРНК в организм.
Попытка Гилбоа стронула настоящую академическую лавину исследований по мРНК и попыток пристроить ее в медицинской сфере.
Хёрр первым добился успеха. Работая в Тюбингенском университете в Германии, в 2000 году он сообщил, что прямые инъекции могут вызывать иммунный ответ у мышей. В том же году он создал свою компанию CureVac.

Ингмар Хёрр на конференции, фото с твиттера ученого
Но тогда мало кто из его коллег или потенциальных инвесторов проявил интерес к его открытию. Так, Хёрр любит рассказывать, что на конференции, где он представлял первые результаты, прямо перед самой трибуной стоял лауреат один Нобелевской премии и говорил: «Что за ахинею вы тут нам несете! Это полный бред!».
Однако Хёрру все же удалось найти финансирование, и уже через несколько лет начались испытания на людях. Ведущий специалист компании Стив Пасколо поступил, как врачи-исследователи «классической» эпохи: он стал первым подопытным и ввел себе мРНК. На ноге у Пасколо до сих пор сохраняются белые шрамы размером со спичечную головку на месте участков, из которых дерматолог взял биопсию на анализ8. Вскоре после этого началось официальное испытание опухолеспецифической мРНК для лечения людей с раком кожи.
Турецкие ученые Угур Шахин и его жена-иммунолог Озлем Тюречи тоже начали изучать мРНК в конце 1990-х, но основали компанию несколько позже, чем Хёрр. Они оттачивали свою технологию в течение многих лет, работая в Университете Йоханнеса Гутенберга в Майнце, получая патенты и исследовательские гранты, занимаясь написанием статей, и только в 2007 году представили коммерческий план инвесторам-миллиардерам. В качестве стартового капитала Шахин получил 150 миллионов евро.
А вот биохимик Каталин Карико и иммунолог Дрю Вайсман, работавшие тогда в Пенсильванском университете в Филадельфии, смогли выбить для своего проекта куда более скромную сумму. Правительство США выделило их стартапу по разработке мРНК под названием «RNARx» более скромную сумму – всего 97 тысяч долларов в виде гранта. Каталин Карико и Дрю Вайсман сделали то, что теперь называют ключевым открытием: оказывается, изменение части кода мРНК помогает синтетической мРНК ускользать от острого глаза иммунитета.
Ключевой прорыв
Все 90-е Карико работала в лаборатории университета над преобразованием мРНК в лекарственную платформу. Грантодатели один за одним отклоняли ее заявки на финансирование, но она не сдавалась. Дела шли так плохо, что в 1995 году после неоднократных отказов ее даже поставили перед выбором: покинуть Пенсильванский университет или согласиться на понижение в должности и сокращение заработной платы. Карико решила остаться и продолжить работу над модификацией протоколов Мэлоуна. В итоге у нее получилось заставить клетки производить большой и сложный белок, имеющий терапевтическое значение.
В 1997 году она начала работать с Вайсманом, который только что открыл лабораторию в Пенсильванском университете. Вместе они планировали разработать вакцину против ВИЧ/СПИДа на основе мРНК. Но мРНК Карико вызывали выраженные воспалительные реакции в экспериментах на мышах.
Вскоре ученые выяснили, в чем дело. Оказалось, что синтетическая мРНК возбуждает так называемые Toll-подобные рецепторы – первую линию иммунного ответа на сигналы опасности от патогенов. В 2005 году Каталин Карико и Дрю Вайсман сообщили, что перестройка химических связей на одном из нуклеотидов мРНК, уридине, которая превращает его в аналог, псевдоуридин, по-видимому, мешает организму идентифицировать мРНК как врага9.
В то время немногие ученые признавали терапевтическую ценность подобных модифицированных нуклеотидов, но после открытия Карико и Вайсмана у научного мира открылись глаза! Уже в сентябре 2010 года группа исследователей под руководством Деррика Росси из Бостонской детской больницы в Массачусетсе, описала, как модифицированные мРНК могут быть использованы для трансформации клеток кожи сначала в эмбрионоподобные стволовые клетки, а затем в сокращающуюся мышечную ткань. Открытие произвело фурор. Журнал «Time» назвал Росси одним из «значимых людей» 2010 года. Именно Деррик Росси стал одним из соучредителем стартапа Moderna – название, сейчас хорошо знакомое каждому.
Moderna пыталась лицензировать патенты на модифицированную мРНК, которые Пенсильванский университет подал в 2006 году на изобретение Карико и Вайсман. Но было слишком поздно. После неудачной попытки заключить лицензионное соглашение с RNARx, Пенсильванский университет предоставил исключительные патентные права небольшому поставщику лабораторных реагентов в Мэдисоне. Компания, которая теперь называется Cellscript, заплатила за сделку всего 300 000 долларов. Теперь Cellscript получает сотни миллионов долларов в качестве сублицензионных сборов от Moderna и BioNTech, создателей первых мРНК-вакцин против COVID-19. Оба продукта содержат модифицированную мРНК.
А RNARx израсходовал еще 800 000 долларов грантов и прекратил существование в 2013 году, примерно в то время, когда Карико присоединилась к BioNTech (сохранив должность преподавателя в Пенсильванском университете).
Другие кандидаты на ключевую роль в создании мРНК-вакцин
Исследователи до сих пор спорят о том, насколько важную роль играет открытие Карико и Вайсмана в создании современных мРНК-вакцин. Moderna всегда использовала модифицированную мРНК: даже ее название – это комбинация этих двух слов, – но ряд компаний обошлись без этой молекулы.
Так, ученые из фармацевтической фирмы Shire в Массачусетсе (которая позже стала частью японской компании Takeda) пришли к выводу, что на основе немодифицированной мРНК тоже можно сделать качественный препарат, если добавить правильные «шапочки» (5cap, обычно не переводится – «головная» область незрелой мРНК, модифицированный гуаниновый нуклеотид) и удалить все примеси.
Shire продала свои разработки Translate Bio, компании из Кембриджа. Теперь Translate Bio создает на ее основе вакцину от COVID-19. И хотя она все еще находится на начальных стадиях клинических испытаний, французский фармгигант Sanofi уже убежден, что технологию ждет успех – в августе 2021 года он объявил о планах приобрести Translate Bio за 3,2 миллиарда долларов.
Помимо этого подхода, есть и еще. Так, CureVac решает вопрос ухода из-под внимания иммунитета путем изменения генетической последовательности мРНК для минимизации количества уридина в вакцинах. Они двадцать лет разрабатывали свою технологию, но когда попытались применить ее для создания мРНК-вакцин от бешенства и от COVID-19, успех оказался сомнительным: данные поздних фаз клинических испытаний испытания показали, что вакцина-кандидат от коронавируса CureVac была намного менее эффективной, чем вакцины Moderna или BioNTech10.
Именно благодаря этим негативным результатам многие ученые склоняются к мысли, что идеи Карико и Вайсмана про замену уридина псевдоуридином – именно то, что помогло мРНК-вакцинам родиться.
Однако есть и голоса против. Например, Suzhou Abogen Biosciences сейчас заканчивает испытания антикоронавирусной вакцины ARCoV, в которой используется немодифицированная мРНК – и промежуточные результаты у нее пока что очень неплохие. Вопрос, единственный ли фактор успеха замена уридина или один из многих, пока что остается открытым.
Примечания
- 1. Cobb M. Who discovered messenger RNA?
- 2. Dimitriadis, G. J. Translation of rabbit globin mRNA introduced by liposomes into mouse lymphocytes
- 3. Ostro, M. J., Giacomoni, D., Lavelle, D., Paxton, W. & Dray, S. Evidence for translation of rabbit globin mRNA after liposome-mediated insertion into a human cell line
- 4. Krieg, P. A. & Melton, D. A. Functional messenger RNAs are produced by SP6 in vitro transcription of cloned cDNAs
- 5. Malone, R. W., Felgner, P. L. & Verma, I. M. Cationic liposome-mediated RNA transfection
- 6. Martinon, F. et al. Induction of virus-specific cytotoxic T lymphocytes in vivo by liposome-entrapped mRNA
- 7. Conry, R. M. et al. Characterization of a messenger RNA polynucleotide vaccine vector
- 8. J Probst 1, B Weide, B Scheel, B J Pichler, I Hoerr, H-G Rammensee, S Pascolo. Spontaneous cellular uptake of exogenous messenger RNA in vivo is nucleic acid-specific, saturable and ion dependent
- 9. Karikó, K., Buckstein, M., Ni, H. & Weissman, D. Suppression of RNA Recognition by Toll-like Receptors: The Impact of Nucleoside Modification and the Evolutionary Origin of RNA
- 10. Kremsner, P. G. Safety and immunogenicity of an mRNA-lipid nanoparticle vaccine candidate against SARS-CoV-2